Capita sempre più spesso di sentir parlare di “microbiota” o “microbioma” intestinale e di come occorra averne cura onde mantenere il corpo in buona salute.
Microbiota o Microbioma?
È necessario fare una distinzione poiché quando ne parliamo ci riferiamo a contenuti differenti.
Con microbiota intestinale si intende l’insieme dei microbi (batteri commensali, lieviti, virus e organismi animali primitivi molto semplici, quali i protozoi) che convivono nell’intestino. Mentre microbioma indica la totalità del patrimonio genetico posseduto dal microbiota, cioè i geni che quest’ultimo è in grado di esprimere.
Il microbiota intestinale umano è costituito da più di 50.000 miliardi di microorganismi appartenenti ad almeno 1000 specie diverse. Scolasticamente il microbiota intestinale viene suddiviso in organismi autoctoni, specie indigene che occupano uno specifico habitat intestinale (mucosa intestinale), e organismi alloctoni, che sono “viaggiatori di passaggio”, presenti occasionalmente nel tratto digerente collegati alla dieta e ad altri fattori ambientali. In umana, un terzo del microbiota è simile nella maggior parte delle persone, mentre per 2/3 è individualmente diverso. Qualcosa di simile accade anche negli animali, inclusi i pesci. Il microbiota viene acquisito alla nascita, quando l’individuo è esposto per la prima volta a specie batteriche presenti nell’ambiente. In seguito si incrementa in quantità e varietà tramite l’esposizione continua all’ambiente e con l’alimentazione.
Nel mondo acquatico, l’acqua è un formidabile veicolo di microorganismi appartenenti a varie specie, così come lo è la catena alimentare, incluso il mangime fornito negli allevamenti. La maggior parte di questi microorganismi non sono dannosi per la salute, anzi, sono benefici perché sono parte di numerosi processi fisiologici. Il microbiota intestinale quindi non è “innato” ma è un “organo acquisito”, ancora molto sconosciuto. Ciò su cui gli studiosi concordano, è che il microbiota sia direttamente relazionato con la salute, con il sistema immunitario, con il funzionamento dell’apparato digerente, con la sensazione di benessere, ecc.
L’asse intestino-cervello
Uno studio di qualche anno fa ha dimostrato che le persone in disbiosi (squilibrio microbico) soffrono più facilmente di problemi di origine nervosa e psicologica, come la depressione e l’ansia anche in forme severe. Anche secondo uno studio dell’Università californiana di Los Angeles, le persone con disturbi gastrointestinali cronici soffrono più facilmente di ansia. Questo perché i microbi intestinali producono anche composti chimici che influenzano il nostro umore, come la serotonina – nota anche come “ormone del buonumore”. Alcuni generi di batteri come i Lactobacillus assunti come probiotici hanno riportato miglioramenti negli stati d’ansia e nell’umore in generale.
Siamo ancora lontani dal comprendere l’esatto funzionamento di questa connessione, ma è certamente chiaro che microbiota intestinale e cervello collaborano al benessere dell’individuo. Con la dieta andiamo ad alimentare i miliardi di batteri che vivono nell’apparato digerente. La varietà e la quantità di microorganismi presenti nel microbiota intestinale (e non solo) è direttamente influenzata dalla diversità alimentare. Si crea una sorta di equilibrio che se alterato può dare origine a diversi disturbi, che vanno dai problemi intestinali alle malattie autoimmuni e croniche. È vero anche che il microbiota viene influenzato e alterato da molte altre cose (come le infezioni, gli antibiotici e i medicinali, ecc.), ma il ruolo dell’alimentazione sembra essere primario.
Siamo ancora lontani dal comprendere l’esatto funzionamento di questa connessione, ma è certamente chiaro che microbiota intestinale e cervello collaborano al benessere dell’individuo. Con la dieta andiamo ad alimentare i miliardi di batteri che vivono nell’apparato digerente. La varietà e la quantità di microorganismi presenti nel microbiota intestinale (e non solo) è direttamente influenzata dalla diversità alimentare. Si crea una sorta di equilibrio che se alterato può dare origine a diversi disturbi, che vanno dai problemi intestinali alle malattie autoimmuni e croniche. È vero anche che il microbiota viene influenzato e alterato da molte altre cose (come le infezioni, gli antibiotici e i medicinali, ecc.), ma il ruolo dell’alimentazione sembra essere primario.
Lo studio del microbiota intestinale negli allevamenti ittici
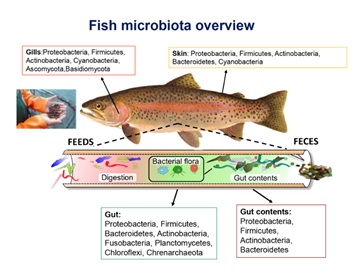 Le evidenze raccolte in questi anni indicano come nel pesce esistano complesse comunità microbiche a livello dei diversi distretti corporei come cute, branchie ed intestino, ovvero a livello di quegli organi che sono a diretto contatto con l’ambiente esterno. Il microbiota della cute e delle branchie riflette quello dell’acqua circostante, mentre il microbiota intestinale è principalmente influenzato dalla dieta. Recenti studi indicano la possibilità di promuovere condizioni ottimali per lo stato di salute e l’equilibro della flora batterica intestinale dei pesci mediante manipolazione della dieta.
Le evidenze raccolte in questi anni indicano come nel pesce esistano complesse comunità microbiche a livello dei diversi distretti corporei come cute, branchie ed intestino, ovvero a livello di quegli organi che sono a diretto contatto con l’ambiente esterno. Il microbiota della cute e delle branchie riflette quello dell’acqua circostante, mentre il microbiota intestinale è principalmente influenzato dalla dieta. Recenti studi indicano la possibilità di promuovere condizioni ottimali per lo stato di salute e l’equilibro della flora batterica intestinale dei pesci mediante manipolazione della dieta.Tra questi gli studi condotti nell’ambito del progetto AGER Fine Feed For Fish (4F) presso l’Università degli Studi dell’Insubria.
Trattandosi di ceppi batterici per la maggior parte non coltivabili su piastra in laboratorio, il metodo di studio prevede l’identificazione di popolazione batteriche cercando frammenti del loro DNA.
Come si analizzano i frammenti di DNA dei batteri?
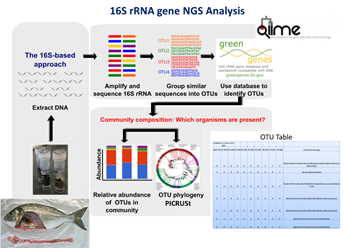 Si analizzano utilizzando tecniche innovative definite Next Generation Sequencing (NGS) che hanno dato un notevole impulso alla caratterizzazione del microbiota umano e della sua complessità che ora vengono applicate anche nello studio del microbiota degli animali, inclusi i pesci. Queste tecniche sono in grado di sfruttare la particolare conformazione della sequenza di acidi nucleici che caratterizza il patrimonio genetico della flora commensale. Si basano sull’amplificazione mediante PCR e sequenziamento di alcune regioni variabili di geni da cui derivano le sequenze di rRNA 16S (16S rDNA, DNA ribosomiale 16S). Tali regioni sono infatti, specie specifiche e il loro sequenziamento, permette di identificare e differenziare le diverse specie batteriche presenti nel tratto intestinale dei pesci.
Si analizzano utilizzando tecniche innovative definite Next Generation Sequencing (NGS) che hanno dato un notevole impulso alla caratterizzazione del microbiota umano e della sua complessità che ora vengono applicate anche nello studio del microbiota degli animali, inclusi i pesci. Queste tecniche sono in grado di sfruttare la particolare conformazione della sequenza di acidi nucleici che caratterizza il patrimonio genetico della flora commensale. Si basano sull’amplificazione mediante PCR e sequenziamento di alcune regioni variabili di geni da cui derivano le sequenze di rRNA 16S (16S rDNA, DNA ribosomiale 16S). Tali regioni sono infatti, specie specifiche e il loro sequenziamento, permette di identificare e differenziare le diverse specie batteriche presenti nel tratto intestinale dei pesci.
 Si analizzano utilizzando tecniche innovative definite Next Generation Sequencing (NGS) che hanno dato un notevole impulso alla caratterizzazione del microbiota umano e della sua complessità che ora vengono applicate anche nello studio del microbiota degli animali, inclusi i pesci. Queste tecniche sono in grado di sfruttare la particolare conformazione della sequenza di acidi nucleici che caratterizza il patrimonio genetico della flora commensale. Si basano sull’amplificazione mediante PCR e sequenziamento di alcune regioni variabili di geni da cui derivano le sequenze di rRNA 16S (16S rDNA, DNA ribosomiale 16S). Tali regioni sono infatti, specie specifiche e il loro sequenziamento, permette di identificare e differenziare le diverse specie batteriche presenti nel tratto intestinale dei pesci.
Si analizzano utilizzando tecniche innovative definite Next Generation Sequencing (NGS) che hanno dato un notevole impulso alla caratterizzazione del microbiota umano e della sua complessità che ora vengono applicate anche nello studio del microbiota degli animali, inclusi i pesci. Queste tecniche sono in grado di sfruttare la particolare conformazione della sequenza di acidi nucleici che caratterizza il patrimonio genetico della flora commensale. Si basano sull’amplificazione mediante PCR e sequenziamento di alcune regioni variabili di geni da cui derivano le sequenze di rRNA 16S (16S rDNA, DNA ribosomiale 16S). Tali regioni sono infatti, specie specifiche e il loro sequenziamento, permette di identificare e differenziare le diverse specie batteriche presenti nel tratto intestinale dei pesci.Questo tipo di analisi prevede l’estrazione del 16S rDNA da matrici complesse, come ad esempio i campioni fecali, l’amplificazione via PCR del gene 16S con l’utilizzo di primer universali e il sequenziamento dell’intera miscela di ampliconi prodotti, in un’unica soluzione. Si generano in questo modo milioni di sequenze le quali sono poi elaborate tramite software dedicati in grado di fare sia un’analisi tassonomica delle sequenze ottenute che un’analisi funzionale del microbioma.
Fonte: Genciana Terova, Marco Saroglia, Università degli Studi dell’Insubria












